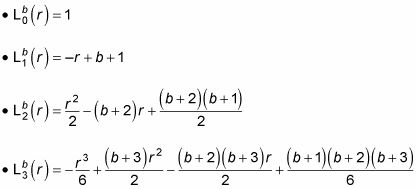Calculer la fonction d'onde d'un atome d'hydrogène utilisant le schr & # 246 équation-Dinger
Si votre instructeur physique quantique vous demande de trouver la fonction d'onde d'un atome d'hydrogène, vous pouvez commencer avec la radiale Schr # 246-Dinger équation, Rnl(r), Qui vous dit que
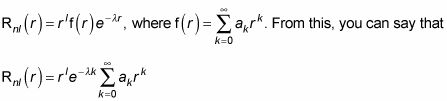
L'équation précédente vient de résoudre le radiale Schr # 246-Dinger équation:
La solution est seulement bon à une constante multiplicative, de sorte que vous ajouter comme une constante, unenl (qui se révèle dépendre du nombre quantique principal n et le nombre quantique de moment angulaire l), comme ça:
Vous trouverez unenl en normalisant Rnl(r).
Maintenant, essayez de résoudre Rnl(r) Par juste à plat de faire le calcul. Par exemple, essayez de trouver R10(r). Dans ce cas, n = 1 et l = 0. Ensuite, parce que N + l + 1 = n, vous avez N = n - l - 1. Donc N = 0 ici. Cela rend Rnl(r) Ressembler à ceci:
Et la sommation de cette équation est égale à
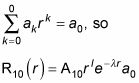
Et parce que l = 0, rl = 1, de sorte que
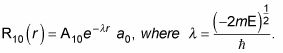
Par conséquent, vous pouvez aussi écrire
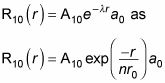
où r0 est le rayon de Bohr. Pour trouver un10 et un0, vous normaliser
à 1, ce qui signifie l'intégration
sur tout l'espace et le réglage du résultat à 1.
et l'intégration des harmoniques sphériques, tels que Y00, sur une sphère complète,
vous donne 1. Par conséquent, vous êtes de gauche avec la partie radiale de normaliser:
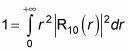
Branchement
en
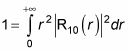
te donne
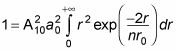
Vous pouvez résoudre ce genre de partie intégrante de la relation suivante:
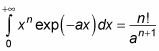
Avec ce rapport, l'équation
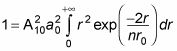
devient
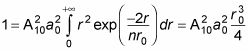
Donc,
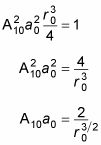
Ce résultat est assez simple. Parce A10 est juste là pour normaliser le résultat, vous pouvez définir une10 à 1 (ce ne serait pas le cas si
plusieurs termes impliqués). Donc,
Cela est très bien, et il rend R10(r), qui est
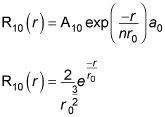
Tu le sais
Et ainsi
devient
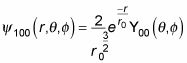
Ouf. En général, voici ce que la fonction d'onde
ressemble à de l'hydrogène:
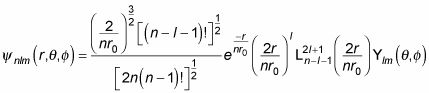
où
est un polynôme de Laguerre généralisé. Voici les quelques premiers polynômes de Laguerre généralisés: