Comment utiliser le principe d'incertitude de Heisenberg par rapport à la position et de l'élan
Les physiciens quantiques comprendre que la matière présente des propriétés comme des vagues, ce qui signifie que la matière, comme des vagues, ne sont pas localisés dans l'espace. Ce fait inspiré Werner Heisenberg, en 1927, à venir avec son célèbre principe d'incertitude.
Vous pouvez tout à fait décrire des objets à la physique classique par leur élan et la position, les deux qui vous permet de mesurer exactement. En d'autres termes, la physique classique est complètement déterministe.
Sur l'échelle atomique, cependant, la physique quantique peint un tableau différent. Ici, la Heisenberg principe d'incertitude dit qu'il ya une incertitude inhérente à la relation entre la position et la vitesse. Dans le X direction, par exemple, il ressemble à ceci:
où
est l'incertitude de mesure dans la particule de X la position,
est l'incertitude de mesure dans son élan dans le X direction et
Cela revient à dire, plus précisément vous connaissez la position d'une particule, moins vous savez précisément l'élan, et vice versa. Cette relation est valable pour les trois dimensions:
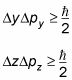
Et le principe d'incertitude de Heisenberg est une conséquence directe de la nature ondulatoire de la matière, parce que vous ne pouvez pas complètement cerner une vague.
La physique quantique, contrairement à la physique classique, est complètement non déterministe. Vous ne pouvez jamais connaître la position précise et dynamique d'une particule à un moment donné. Vous pouvez donner que des probabilités pour ces mesures liées.






