La théorie des cordes et le modèle atomique
Voici une brève exploration du modèle standard de la physique des particules et comment il se rapporte à la théorie des cordes. Toute la théorie des cordes complète devra inclure les caractéristiques du modèle standard et aussi aller au-delà pour inclure gravité ainsi.
Aujourd'hui, les scientifiques savent que ces atomes ne sont pas, comme les Grecs imaginaient, les plus petits morceaux de matière. Les scientifiques vite rendu compte que les atomes avaient plusieurs pièces à l'intérieur d'eux:
Électrons chargés négativement encerclant le noyau
Noyau chargé positivement
Les particules qui composent le noyau (elle est composée de petits morceaux, aussi) et des électrons sont parmi les particules, avec plusieurs autres, que le modèle standard de la physique des particules, explique, et, finalement, que la théorie des cordes devraient également expliquer.
Découvrir l'électron
La électron est une particule chargée négativement contenue dans l'atome. Il a été découvert en 1897 par le physicien britannique JJ Thomson, si les particules chargées (y compris le nom “ électrons ”) avaient été émis l'hypothèse plus tôt.
Certains physiciens avaient déjà émis l'hypothèse que les unités de la charge pourraient être circulant autour dans les appareils électriques. (Benjamin Franklin a proposé une telle idée dès les années 1700.) Technologie seulement rattrapé cette idée dans les années 1800, avec la création du tube cathodique, représenté sur cette figure.
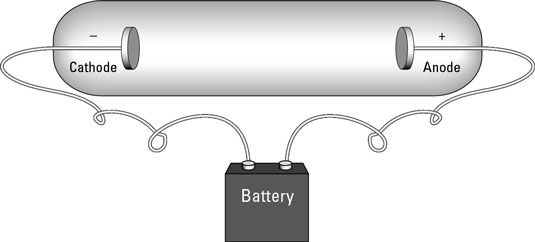
Dans un tube à rayons cathodiques, une paire de disques métalliques est connectée à une batterie. Les disques métalliques sont placés dans un tube de verre scellé contenant pas d'air - un tube à vide. La tension électrique provoque une des plaques de métal à devenir chargée positivement (un anode) Et la personne à devenir chargé négativement (la cathode, d'où le dispositif tire son nom). Tubes cathodiques sont à la base de tubes de télévision et de moniteurs d'ordinateur traditionnels.
Lorsque le courant électrique a été allumé, le tube serait de commencer à vert. En 1897, Thomson était à la tête du laboratoire Cavendish à Cambridge, en Angleterre, et a entrepris de vérifier les propriétés de ce tube cathodique lueur. Il a découvert que la lueur était dû à un faisceau de particules chargées négativement volants entre les plaques.
Ces particules chargées négativement sont venus plus tard d'être appelé électrons. Thomson a également compris que les électrons étaient incroyablement léger - 2000 fois plus léger qu'un atome d'hydrogène.
Thomson non seulement découvert l'électron, mais il a théorisé que l'électron a fait partie de l'atome (atomes ne sont pas une idée complètement accepté à l'époque) qui en quelque sorte a obtenu frappé libre de la cathode et coulait dans le vide à l'anode. Avec cette découverte, les scientifiques ont commencé découvrir façons d'explorer l'intérieur des atomes.
Le noyau est la chose dans le milieu
Au centre de l'atome est une bille dense de la matière, appelée noyau, avec une charge électrique positive. Peu de temps après électrons ont été découverts, il est devenu clair que si vous avez extrait un électron d'un atome, l'atome a été laissé avec une charge électrique légèrement positif.
Pendant un certain temps, l'hypothèse était que l'atome était une masse chargée positivement qui contenait électrons négatifs à l'intérieur, comme des morceaux de fruits chargé négativement dans un gâteau aux fruits chargé positivement. L'ensemble du gâteau aux fruits serait neutre à moins que vous avez extrait des fruits de celle-ci.
En 1909, cependant, une expérience de Hans Geiger et Ernest Marsden, travaillant sous Ernest Rutherford, a contesté cette image. Ces scientifiques ont tiré des particules chargées positivement à une mince feuille d'or. La plupart des particules traversa la feuille, mais à chaque fois dans un moment l'un d'eux a rebondi fortement.
Rutherford a conclu que la charge positive de l'atome d'or n'a pas été répandu dans l'atome dans le modèle de gâteau aux fruits, mais a été concentrée dans un petit noyau chargé positivement, et que le reste de l'atome était vide. Les particules qui rebondissent étaient ceux qui ont frappé ce noyau.



