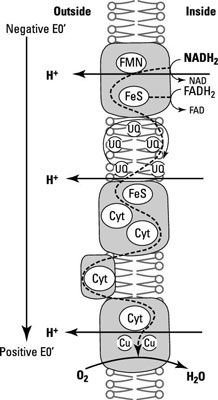
Respiration et électrons transporteurs
La répartition des composés par la respiration de presse beaucoup plus d'énergie que la répartition des mêmes composés par fermentation. En effet, la réduction complète des produits de fermentation est impossible sans oxygène ou de l'oxygène à des substituts agissent comme accepteurs d'électrons terminal.
La star de ce phénomène est le chaîne de transport d'électrons, qui implique plusieurs accepteurs d'électrons positionnés à l'intérieur d'une membrane dans le but de réduire la puissance de sorte que les plus faibles accepteurs d'électrons sont à une extrémité de la chaîne et les accepteurs d'électrons sont les plus forts à l'autre extrémité. Il est l'orientation spécifique de porteurs d'électrons dans la membrane qui crée la force motrice protonique et relie la synthèse d'ATP avec elle.
La chaîne de transport d'électrons réduit composés organiques à CO2 et conserve une partie de l'énergie que les électrons sont transférés à partir du substrat de carbone (glucose), par l'intermédiaire de plusieurs réactions d'oxydoréduction à l'accepteur d'électrons terminal (O2).
Certains transporteurs membranaires, comme les quinones, sont des molécules non protéiques, mais la plupart sont des enzymes d'oxydation-réduction et certains d'entre eux ont des groupes prosthétiques qui participent à des réactions d'oxydoréduction. Des groupes prosthétiques sont de petites molécules qui sont liées de façon permanente à une enzyme et sont importants pour son activité.
Après sont nombreux transporteurs d'électrons différents qui participent à la chaîne de transport d'électrons:
Déshydrogénases NADH: Ce sont des protéines qui acceptent un électron (e-) Et d'un proton (H+) À partir de NADH, NAD à ce oxydant+ et de les transmettre sur un flavoprotéine.
Flavoprotéines: Ceux-ci sont constitués d'une protéine liée à un groupe prosthétique appelée Flavin, qui provient de la vitamine riboflavine. Le groupe de Flavin accepte deux e- et deux H+ mais seulement fait don de deux e- lorsqu'il est oxydé.
Cytochromes: Ces protéines contiennent un groupe prosthétique hème avec un atome de fer dans son centre qui gagne ou perd un seul e-. Il existe différentes catégories de cytochromes en fonction du type de l'hème qu'ils contiennent et marquées avec une lettre différente (par exemple, le cytochrome a). Lorsque la même classe de cytochrome est légèrement différent dans deux organismes, chacun obtient un nombre associé à ce nom (par exemple, un cytochromes1 et un2).
Protéines fer-soufre: Ceux-ci lient fer, mais sans groupe hème. Au lieu de cela, ils ont des groupes d'atomes de soufre et de fer disposée au centre de la protéine. Ils acceptent que e- et ont une gamme de réduction de la puissance en fonction du nombre d'atomes de fer et du soufre présents.
Quinones: Ces molécules hydrophobes (et non des protéines) sont libres de se déplacer autour de la membrane. Ils acceptent de deux e- et deux H+ et généralement agir comme un lien entre les protéines et les cytochromes fer-soufre.
Ici, vous pouvez voir des exemples de certains de ces composés et comment ils sont physiquement assis à l'intérieur de la membrane dans le bon ordre pour les électrons de circuler de la plus électronégatif à la plus électropositif.