Le maintien d'un système à pression constante: le processus isobarique
En physique, quand vous avez un processus où la pression reste constante, il est appelé isobare (Baric moyens “ pression ”). La première figure montre un exemple d'un système isobare, où un cylindre avec un piston est soulevé par une quantité de gaz que le gaz devient plus chaud. Le volume du gaz est en train de changer, mais le piston pondérée maintient la pression constante.
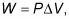
Graphiquement, vous pouvez voir ce que le processus isobarique ressemble dans la deuxième figure, où le volume est en train de changer alors que la pression reste constante. Car # 8232;
le travail est la zone ombragée sous le graphique.
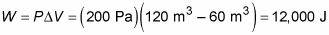
Disons que vous avez 60 mètres cubes d'un gaz parfait à une pression de 200 pascals. Vous chauffer le gaz jusqu'à ce qu'elle se développe pour un volume de 120 mètres cubes. Combien de travail ne le gaz faire? Tout ce que vous avez à faire est de brancher les numéros:
Le gaz fait 12.000 joules de travail comme il se dilate sous pression constante.
Voici un autre exemple: Supposons que vous êtes en attente pour un vol de correspondance à la prochaine conférence de la physique. Vous regardez autour, mais ne voyez pas beaucoup à vous amuser avec - juste une fontaine d'eau. Prouver que les physiciens peuvent trouver du plaisir partout, vous prenez un gramme d'eau de la fontaine et de le mettre dans la chambre isobarique de poche qui vous arrive toujours à transporter avec vous. Comme un garde de sécurité de l'aéroport regarde, vous augmentez la pression
et augmenter la température de l'eau de 62 degrés Celsius.
Vous constatez que le gramme de l'eau augmente en volume
“ Hmm, ” tu penses. “ je me demande ce que le travail a été fait par l'eau et ce que la variation d'énergie interne de l'eau était le ”. Le processus était isobarique, de sorte que le travail accompli par l'eau était
Combler les numéros et de faire les rendements de mathématiques:
Voilà donc le travail accompli par l'eau. Que dire de la variation de l'énergie interne de l'eau? La première loi de la thermodynamique vous dit que
Tu sais W, mais ce qui est Q? Q est la chaleur absorbée par l'eau. Vous savez que le changement de température de l'eau, et l'utilisation de la capacité thermique spécifique de l'eau, vous pouvez trouver la chaleur effectivement absorbée par l'eau en utilisant cette équation:
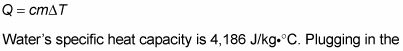
numéros et faire le calcul vous donne
Maintenant, revenons à la première loi de la thermodynamique:
En substituant les valeurs que vous donne la variation de l'énergie interne:
Hmm, vous pensez. Le travail accompli était un petit 0,002 joules, tandis que la variation de l'énergie interne était de 260 joules. Intéressant - très peu de travail a été fait parce que l'eau n'a pas augmenté beaucoup, mais vous avez vu un gain juste de l'énergie interne, car la température de l'eau a augmenté.






