Un problème de mécanisme de chimie organique exemple
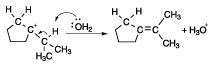
Supposons que vous travaillez d'une cession de la chimie organique, et vous êtes invité à proposer un mécanisme pour la conversion de l'alcool indiqué sur la figure ci-dessous pour l'alcène représenté sur la même figure.
D'abord, vous voulez identifier quel genre de mécanisme que vous avez affaire. Est-il un acide ou un mécanisme de base? Est-ce un nucléophile ou un mécanisme de électrophile? Est-il un mécanisme de radicaux libres? Parce que le réactif est l'acide sulfurique (H2AINSI4) Plus # 8710- (un symbole qui indique que le mélange réactionnel est chauffé), la réaction sera une réaction acide.
Deuxièmement, déterminer où vous allez dans le mécanisme. Conversion d'un alcool dans un alcène implique généralement la déshydratation (perte d'eau). Mais vous pouvez remarquer que l'alcène dans le produit est dans une position inhabituelle, car la déshydratation met généralement l'alcène adjacent à l'alcool de départ. Le produit dans ce cas a la double liaison un atome de carbone plus loin de sa position attendue. Donc, vous pourriez vous attendre quelque chose d'inhabituel dans ce mécanisme qui explique la régiochimie inhabituel de la réaction.
Maintenant que vous savez à peu près où vous allez dans ce mécanisme, vous pouvez commencer à proposer une voie pour y arriver. Dans un mécanisme d'acide, la première chose que vous voulez à rechercher est un site sur la molécule qui peut être protoné. Le seul site de base sur le matériau de départ dans ce cas est l'alcool, de sorte que la première étape serait de protonation du groupe de l'alcool par l'acide sulfurique.
La première étape de mécanismes acide est presque toujours protonation.
Comme toujours, suivez les conventions de flèche poussant, tirant des flèches pleines tête des électrons à l'endroit où ils vont. (Les seuls mécanismes qui utilisent flèches monoparentales sont des mécanismes anti-radicaux libres.)
Parce que de nombreux professeurs de chimie organique sont convaincus que le cercle intime de l'enfer de Dante est réservé pour les étudiants qui attirent constamment protonation de manière incorrecte, assurez-vous de toujours tirer la flèche des électrons sur la base pour le proton acide que les électrons attaquent. Ne jamais commettre le péché impardonnable de tirer une flèche d'un acide H +. Aussi, pour faire en suivant le mouvement des atomes et des charges plus faciles, les atomes sur les parties de la molécule que le changement dans la réaction sont tirées explicitement avec la structure complète de Lewis, comme le montre la figure suivante.
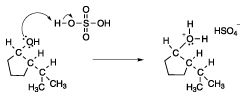
Ensuite, examiner les conséquences de la protonation. Que pouvez-vous faire maintenant que vous ne pouviez pas avant? Une chose que vous pouvez faire maintenant ce que l'alcool est protoné est de former un carbocation. Bien que l'ion hydroxyde, OH-, est un mauvais groupe partant (bases fortes sont de mauvais groupes partants), l'eau est un bon groupe partant. Donc, comme dans un mécanisme typique de déshydratation de l'alcool, l'étape suivante implique la perte de l'eau pour créer un carbocation secondaire, comme représenté sur la figure suivante.
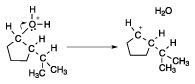
Dans la déshydratation de l'alcool, alors que le carbocation est formé, l'étape suivante est généralement la formation de la double liaison en éliminant un proton. Le faire à cette étape, cependant, serait de former la double liaison dans la mauvaise position. D'une certaine manière, le carbocation besoin de se déplacer de sorte que lorsque l'hydrogène est éliminé, la double liaison est formée dans la position correcte.
Sur une inspection plus minutieuse, vous pouvez remarquer que le carbocation est situé à côté d'un centre de carbone tertiaire. Le carbocation est actuellement un carbocation secondaire, mais il veut vraiment devenir un carbocation tertiaire. (Carbocations tertiaires sont plus stables que les carbocations secondaires.) Un processus de réflexion plus pragmatique pourrait être que ceci est où le cation doit déplacer vers afin d'obtenir l'élimination à la bonne place. Pour obtenir le carbocation en position tertiaire, vous effectuez un déplacement d'hydrure, qui se déplace l'atome d'hydrogène tertiaire et les deux électrons dans la liaison CH au centre de cations, laissant le carbone tertiaire avec la charge positive. Cette étape est montré dans la figure suivante.
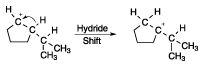
Or, l'élimination d'un proton conduit à la bonne alcène. La déprotonation est montré dans la figure suivante, en utilisant l'eau pour régénérer une molécule d'acide. Vous pouvez également utiliser la base conjuguée de l'acide sulfurique comme base ici.